Oxy là một trong những nguyên tốc vô cùng quan trọng trên trái đất. Tất cả các sinh vật đều cần oxy để phục vụ cho quá trình hô hấp, sinh trưởng. Oxy chính là khởi nguyên của sự sống trên trái đất này. Ngoài phục vụ mục đích tự nhiên, oxy còn được điều chế để phục vụ các hoạt động chuyên sâu hơn trong cuộc sống con người. Điều chế oxi trong phòng thí nghiệm ra sao? làm sao thu được nhiều oxy nhất có thể?
Nội dung bài viết
Oxy là nguyên tố gì? Tính chất vật lý, tính chất hóa học của Oxi
Oxy là một nguyên tố chiếm phần lớn khối lượng vỏ trái đất, lên tới gần 50%. Đây là một nguyên tố phi kim phản ứng cực kỳ mạnh với các nguyên tố khác sinh ra nhóm oxit. Ở điều kiện thường, oxy sẽ tồn tại ở thể khí, len lỏi tự do trong bầu khí quyển. Một số tồn tại trong các hợp chất chứa oxy, ngoài ra thì nó còn tồn tại trong khí quyển.

Oxy tồn tại rất nhiều trong khí quyển
Tính chất vật lý của oxy
Khí oxy là một chất khí không màu, không vị, không mùi, ít tan trong nước, nặng hơn không khí (lý do vì sao càng lên cao thì không khí càng loãng, con người càng khó thở). Oxy sẽ hóa thành dạng lỏng ở nhiệt độ -1830C.
Cấu tạo: 1s22s22p4
Số hiệu nguyên tử trong bảng tuần hoàn nguyên tố hóa học là 8, nguyên tử khối là 16 đvC, thuộc nhóm VIA và chu kì 2.
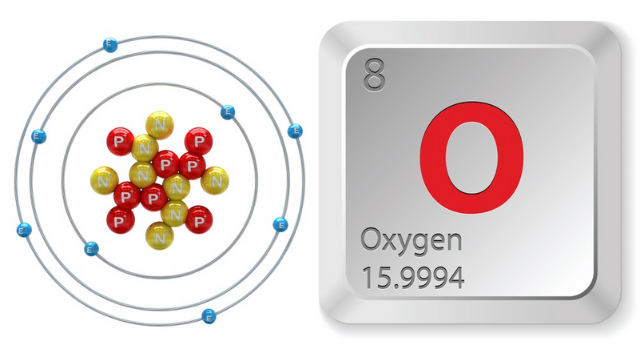
Cấu tạo nguyên tử của oxi
Tính chất hóa học của oxy
Các tính chất hóa học cơ bản của oxy gồm có:
– Oxi tác dụng với kim loại: Phản ứng oxi tác dụng với kim loại diễn ra nhanh chóng trong môi trường có nhiệt độ cao. Nó có thể phản ứng với hầu hết các kim loại, trừ vàng.
Đốt cháy sắt trong oxi: 2O2 + 3Fe → Fe3O4 (hỗn hợp còn có FeO và Fe2O3)
Nung canxi: O2 + 2Ca → 2CaO (phản ứng tại các lò làm vôi)
Đốt Crom trong oxi: 3O2 + 4Cr → 600oC 2Cr2O3
– Oxi tác dụng với phi kim: Ngoài tác dụng với kim loại thì oxy còn có thể kết hợp với một số phi kim khác như:
Phản ứng của oxi và hidro trong môi trường nhiệt độ cao: O2 + 2H2 → 2H2O
Đốt Cacbon (than) trong khí oxy: O2 + C → CO2
Đốt Phốt pho trong khí oxy: 5O2 + 4P→ 2P2O5
– Oxi tác dụng với các chất khác: Oxi còn có thể tác dụng với các hợp chất, sinh ra nhiều chất, hợp chất mới.
2SO2 + O2 → 2SO3
2N2+ 5O2 + 2H2O → 4HNO3
3O2 + CS2 → CO2 + 2SO2
4FeCl2 + O2 + 4HCl → 4FeCl3 + 2H2O
2Fe + O2 + 2H2O → 2Fe(OH)2
C5H12O2 + 7O2 → 5CO2 + 6H2O
BaO4+ 4H2O → Ba(OH)2 + 3H2O2
Hướng dẫn điều chế oxi trong phòng thí nghiệm
Như đã nói ở trên, khí oxy tồn tại rất nhiều trong cuộc sống, trong các hợp chất hóa học. Vì thế việc điều chế oxi trong phòng thí nghiệm khá đơn giản. Chủ yếu trong các bài giảng hóa học cấp phổ thông, chúng ta có thể điều chế oxi trong phòng thí nghiệm dựa vào các cách dưới đây:
Nhiệt phân hợp chất giàu oxi Kali Pemanganat (KMnO4) và Kali Clorat (KClO3).
Phương trình nhiệt phân Kali Pemanganat (KMnO4):
2KMnO4 (t°) → K2MnO4 + MnO2 + O2
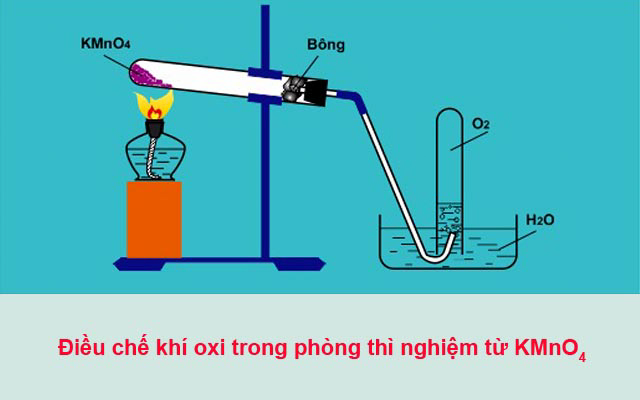
Điều chế oxi trong phòng thí nghiệm từ kmno4
Phương trình đun nóng Kali Clorat (KClO3):
2KClO3 (t°) → 2KCl + 3O2 ( xúc tác là mangan(IV) oxit)
Từ hai phản ứng này, chúng ta sẽ thấy rõ khí oxi thoát ra bằng cách thử đưa tàn đóm đỏ lại gần, môi trường giàu oxy sẽ khiến tàn đóm đỏ bùng cháy lên.
||Xem thêm: Phương Trình Điều Chế HCl Trong Phòng Thí Nghiệm
Các phương pháp thu oxi khi điều chế oxi trong phòng thí nghiệm
Trong hai cách điều chế oxi trong phòng thí nghiệm trên, nếu cứ đốt Kali Pemanganat (KMnO4) và Kali Clorat (KClO3) trong không khí thì khó có thể thu lại được oxy rõ ràng. Chúng ta khi thí nghiệm cần thực hiện thêm phương pháp dưới đây để thu lại oxy.
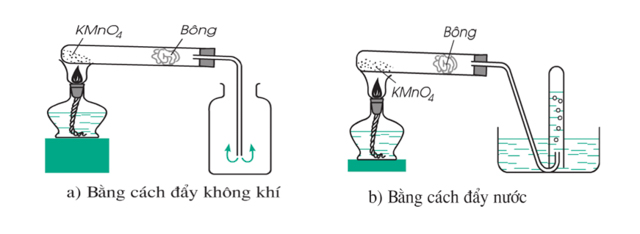
Cách để thu được khí oxi trong thí nghiệm
Để thực hiện phương pháp đẩy nước, chuẩn bị một khay nước, một ống nghiệm, đường dẫn ống,… Cho đầy nước vào ống nghiệm, đưa đầu thoát khí oxy vào trong miệng ống nghiệm. Khí oxy khi bị nhiệt phân ra sẽ có độ tinh khiết cao và được thu vào lòng ống.
Ngoài cách điều chế oxi trong phòng thí nghiệm thì hiện nay để tiết kiệm chi phí, người ta thường điều chế oxy theo kiểu công nghiệp bằng cách điện phân nước hoặc hóa lỏng không khí.
Oxy là một chất có độ quan trọng cực cao đối với cuộc sống. Ngoài cần oxy hít thở hàng ngày thì con người còn cần sử dụng oxy trong y tế, công nghiệp luyện kim, công nghiệp hàn, sản xuất rượu,…Đây là nguyên tố rất quan trọng, có ý nghĩa thực tiễn cực kỳ cao.
||Tham khảo: Cách điều chế nước javen trong phòng thí nghiệm
Với giải đáp trên, bạn đã nắm được cách điều chế oxi trong phòng thí nghiệm rồi chứ. Hóa học là bộ môn rất thú vị, giúp bạn khám phá ra nhiều điều tuyệt vời trong cuộc sống đó.
||Bài viết liên quan khác:
- Điều Chế Clo Trong Phòng Thí Nghiệm | Phương trình, sơ đồ
- Điều Chế HNO3 Trong Phòng Thí Nghiệm | Sơ đồ, phương trình
- Điều Chế SO2 Trong Phòng Thí Nghiệm | Sơ đồ, phản ứng
- Phương Trình Điều Chế HCl Trong Phòng Thí Nghiệm
- Kim Loại Là Gì? Tính Chất Hóa Học Chung Của Kim Loại