Các hợp chất hóa học hữu cơ ngoài việc có trong tự nhiên thì chúng ta có thể điều chế chúng ở trong phòng hóa học hoặc trong công nghiệp. Nếu muốn điều chế C2H2, chúng ta cần phải thực hiện các phản ứng nào? điều chế axetilen trong phòng thí nghiệm có dễ không?
Nội dung bài viết
Tìm hiểu về tính chất vật lý của Axetilen (C2H2)
Axetilen là một trong những hợp chất hữu cơ ở dạng thể khí, không mùi, không màu, ít tan được trong nước. Khí C2H2 đo được có trọng lượng nhẹ hơn không khí (dC2H2/kk = 26/29).
Công thức cấu tạo của hợp chất ở dạng phân tử: (H-C = C-H), viết gọn (HC = CH). Nhìn vào công thức cấu tạo chúng ta có thể nhận thấy hợp chất hữu cơ này ở dạng có liên kết ba. Đây là một dạng liên kết không bền, dễ dàng bị đứt ra trong các phản ứng hóa học.
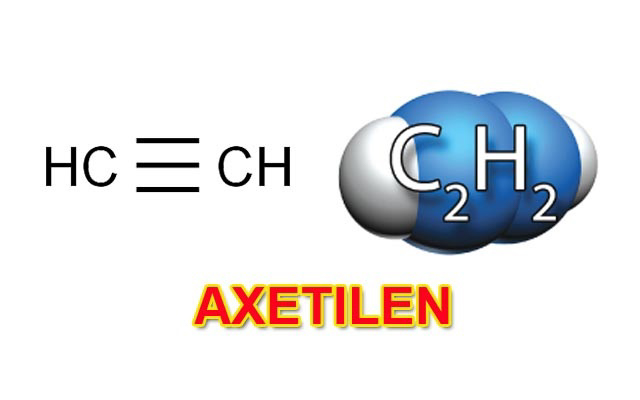
Công thức của axetilen
- Nhiệt độ nóng chảy của C2H2: – 80,8 °C
- Nhiệt độ sôi của C2H2: – 84°C
- Khối lượng riêng của C2H2: 1,097 kg/m3
Tìm hiểu về tính chất hóa học của axetilen (C2H2)
Axetilen là một trong những hợp chất hữu cơ có nhiều phản ứng hóa học xảy ra ở cả điều kiện thường và điều kiện có chất xúc tác. Các phản ứng như: Phản ứng cháy, phản ứng cộng, phản ứng hidrat hóa, phản ứng trùng hợp.

Các phản ứng hóa học của axetilen rất đa dạng
Phản ứng cháy của khí axetilen (C2H2)
Khi axetilen (C2H2) cháy sẽ kết hợp với oxi trong không khí tạo ra khí cacbonic và hơi nước. Phương trình hóa học của phản ứng cháy axetilen (C2H2) như sau:
2C2H2 + 5O2 (t°) → 4CO2 + 2H2O
Phản ứng cộng của khí axetilen (C2H2)
Axetilen (C2H2) có thể phản ứng cộng với nhiều chất như: axit, muối để tạo thành các chất mới. Phương trình hóa học cụ thể:
HC≡CH + Br–Br → Br–CH=CH–Br
Br–CH=CH–Br + Br–Br → Br2CH–CHBr2
HC≡CH + HBr → CH2=CHBr
HC≡CH + AgNO3 + NH3 + H2O → Ag–C≡C–Ag ↓ màu vàng + NH4NO3
Phản ứng trùng hợp của axetilen (C2H2)
Các phân tử axetilen (C2H2) có thể trùng hợp để tạo thành dạng polime với các sợi dài. Phương trình hóa học:
nHC≡CH (t°, xt, p) → (–HC=CH–)n
Phản ứng hidrat hóa của axetilen (C2H2)
Axetilen (C2H2) còn có phản ứng hidrat hóa, xóa liên kết ba trong phân tử để tạo thành sản phẩm axit axetic. Sơ đồ phản ứng như sau:
HC≡CH + H2O (H2SO4) → H–CH=CH–H → CH3COOH
Điều chế axetilen trong phòng thí nghiệm như thế nào?
Để điều chế axetilen trong phòng thí nghiệm, chúng ta có rất nhiều cách khác nhau. Cụ thể cách tiến hành điều chế axetilen trong phòng thí nghiệm:
Chúng ta tiến hành sử dụng một vài mẩu nhỏ chất canxi cacbua (CaC2). Sử dụng một ống nghiệm khoảng 10ml, rót vào trong đó 1ml nước cất, bỏ vào đó canxi cacbua (CaC2) và đậy nắp lại. Phản ứng giữa canxi cacbua (CaC2) và nước sẽ sinh ra khí axetilen (C2H2). Tách chiết khí từ phản ứng bằng ống có đầu vuốt nhọn.
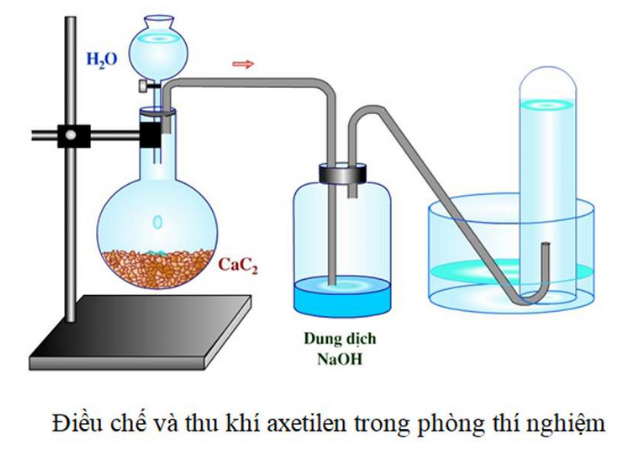
Điều chế axetilen trong phòng thí nghiệm
Phương trình phản ứng hóa học tạo ra axetilen (C2H2):
CaC2 + 2H2O → C2H2 + Ca(OH)2
Axetilen (C2H2) ở phản ứng này được đánh giá còn bị lẫn khá nhiều tạp chất do trong quá trình phản ứng sinh ra nhiều nhiệt.
Ngoài điều chế axetilen trong phòng thí nghiệm, hiện nay chúng ta có thể điều chế bằng các phương pháp công nghiệp. Điều chế theo phương pháp công nghiệp thu được axetilen (C2H2) tinh khiết hơn.
Điều chế axetilen trong công nghiệp bằng cách:
Cho canxi cacbua tác dụng với nước: CaC2 + 2H2O → C2H2 + Ca(OH)2
Phản ứng giữa bạc cacbua với axit: 2HCl + Ag2C2 → 2AgCl + C2H2
Điều chế axetilen từ etilen: CH2=CH2 + Cl2 → Cl-CH2-CH2-Cl
Cl-CH2-CH2-Cl + 2NaOH → CH = CH + 2NaCl + H2O
Điều chế axetilen từ metan: 2CH4 → C2H2 + 3H2
Điều chế axetilen bằng cách cho cacbon phản ứng với hiđro: C + H2 → C2H2
||Tham khảo bài viết:
- Magie Sunfat là chất gì? MgSO4 có kết tủa không? Màu gì?
- Bari Clorua là gì? BaCl2 có kết tủa không? Kết Tủa Màu gì?
Ứng dụng của axetilen (C2H2) trong thực tế

Ứng dụng của axetilen trong thực tế
Trong thực tế, axetilen (C2H2) có rất nhiều ứng dụng tích cực, phục vụ quá trình sản xuất hàng hóa. Cụ thể một số ứng dụng của axetilen (C2H2) gồm:
- Ứng dụng sản xuất cao su, nhựa PVC
- Làm nhiên liệu trong đốt đèn xì, hàn cắt kim loại
- Sản xuất axit axetic
- Sản xuất rượu etylic
Với các diễn giải trên, bạn đọc đã nắm được các tính chất, ứng dụng, cách điều chế axetilen trong phòng thí nghiệm cụ thể rồi chứ. Hóa học là một bộ môn chuyển đổi giữa các chất rất thú vị. Chúc các bạn sớm học tốt môn này nhé!
||Tham khảo bài viết:









